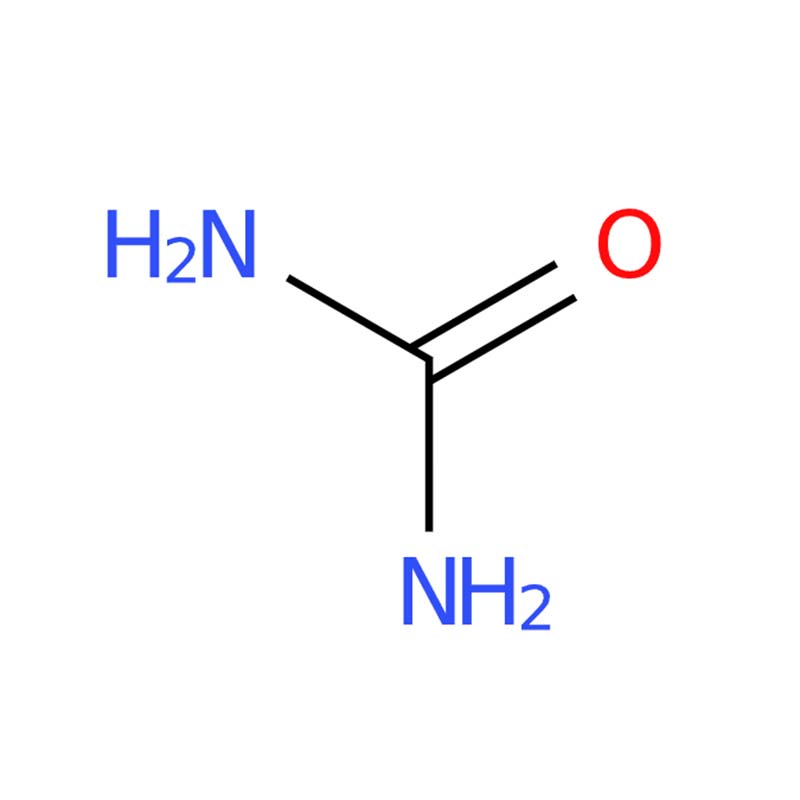
Мочевина
Молекулярная структура:Мочевина имеет плоскую кристаллическую структуру, в которой атомы азота имеют пирамидальную геометрию в конформации с минимальной энергией в газовой фазе, что лежит в основе ее отличительного физико-химического поведения.
Водородные связи:В твердом состоянии кислородный центр мочевины вступает в две водородные связи N-H-O, создавая плотную и стабильную сеть водородных связей, которая повышает общую стабильность молекулы.
Высокая растворимость в воде:Мочевина обладает высокой растворимостью в воде, что объясняется ее способностью образовывать множественные водородные связи с молекулами воды, что делает ее чрезвычайно полезной в промышленных и химических процессах.
Химическое соединение:Атом углерода в мочевине находится в состоянии sp²-гибридизации, а его связи C–N имеют ярко выраженный характер двойной связи, что обуславливает его химическую активность и широкое применение в синтетических целях.
МочевинаМолекула демонстрирует плоскую молекулярную структуру в кристаллической форме, тогда как ее атомы азота принимают пирамидальную геометрию в структуре газовой фазы при минимальной энергии. Эта двойная структурная особенность закладывает основу для различных свойств молекулы. Когда мочевина находится в твердом состоянии, ее атом кислорода образует две водородные связи N-H-O — этот процесс создает плотную, энергетически выгодную сеть водородных связей. Эта сеть, вероятно, нарушает оптимальную молекулярную упаковку, что, в свою очередь, приводит к открытой структуре с лентами, образующими туннели с квадратным поперечным сечением.
Атом углерода в мочевине находится в состоянии sp²-гибридизации, что придаёт его связям C-N характер выраженной двойной связи; кроме того, карбонильный атом кислорода в мочевине имеет более основную природу, чем в таких соединениях, как формальдегид. Высокая растворимость мочевины в воде обусловлена её способностью образовывать обширные водородные связи с молекулами воды, что делает её чрезвычайно полезной в различных промышленных и химических областях.
Химические свойства мочевины
Температура плавления |
132-135 °С(лит.) |
Точка кипения |
332,48°C (оценка) |
плотность |
1,335 г/мл при 25 °C (лит.) |
давление пара |
<0,1 гПа (20 °C) |
показатель преломления |
n20/D 1.40 |
температура хранения |
2-8°С |
растворимость |
H2O: 8 M при 20 °C |
форма |
пудра |
пка |
0,10(при 25℃) |
цвет |
белый |
Удельный вес |
1.335 |
Запах |
почти без запаха |
PH |
8,0-10,0 (20℃, 8M в H2O) |
Растворимость в воде |
1080 г/л (20 ºC) |
λмакс |
λ: 260 нм Aмакс: 0,03 |
Мерк |
14,9867 |
БРН |
635724 |
Диэлектрическая проницаемость |
3.5 (Окружающая среда) |
Стабильность |
Вещества, которых следует избегать, включают сильные окислители. Беречь от влага. |
ИнЧИКей |
AXSQKJJFZKRTKHVVISN |
ЛогП |
-1.660 (восток) |
Справочник по базе данных CAS |
57-13-6 (Справочник базы данных CAS) |
Справочник по химии NIST |
Мочевина (57-13-6) |
Система реестра веществ Агентства по охране окружающей среды |
Мочевина (57-13-6) |
Информация о безопасности
Коды опасности |
Хн,Си |
Заявления о рисках |
36/37/38-40-38 |
Заявления о безопасности |
26-36-24/25-37 |
читатель |
Не регулируется |
WGK Германия |
1 |
RTECS |
6250000 йен |
TSCA |
Да |
Код ТН ВЭД |
31021010 |
Данные об опасных веществах |
57-13-6 (Данные об опасных веществах) |
Токсичность |
LD50 при пероральном приеме у кроликов: 8471 мг/кг LD50 при кожном приеме у крыс 8200 мг/кг |
Мочевинадействует как регулятор выделения азота в физиологии млекопитающих. Синтезируется в печени как побочный продукт при расщеплении белков и в конечном итоге выводится с мочой. Он также встречается в природе в коже, где выполняет двойную функцию: смягчающего средства и мочегонного средства. На практике мочевина используется для денатурации белков и действует как мягкий солюбилизирующий агент для нерастворимых или денатурированных белков. Она особенно ценна для ренатурации белков из образцов, которые ранее были обработаны 6 М гуанидинхлоридом для индукции денатурации, например, телец включения. Мочевину также можно использовать в паре с гуанидингидрохлоридом и дитиотреитолом (ДТТ) для восстановления денатурированных белков до их нативных или активных форм посредством рефолдинга.